Směrnice o kybernetické bezpečnosti
Nařízení o zdravotnických prostředcích
Nařízení o zdravotnických prostředcích pro in vitro diagnostiku
Systém managementu kvality
Systém environmentálního managementu
Systém environmentálního managementu
Interpretace požadavků MDR, IVDR, GMP a dalších regulací s ohledem na specifika farmaceutického odvětví.
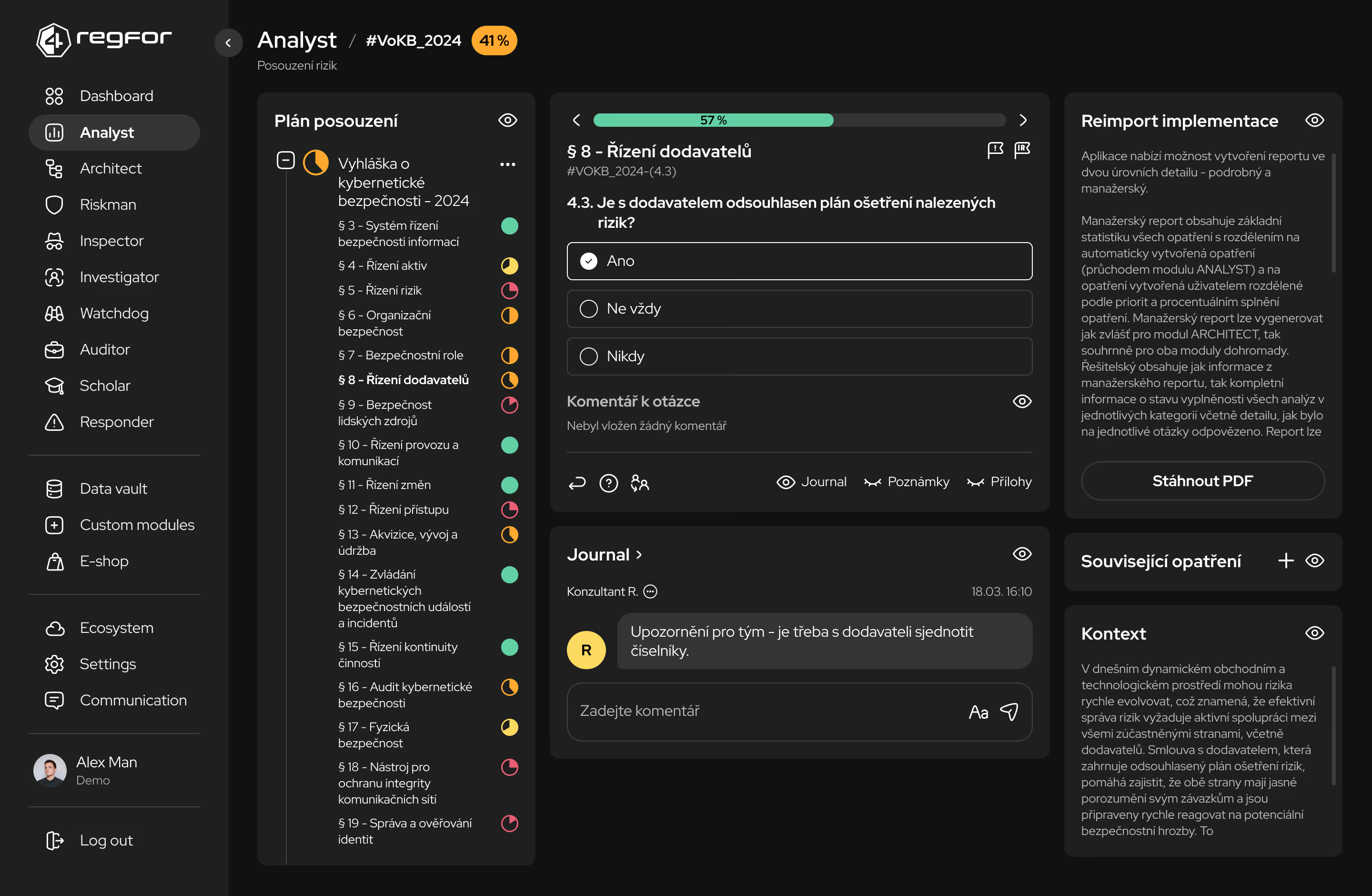
Systematické plánování a sledování implementace opatření podle regulatorních požadavků.
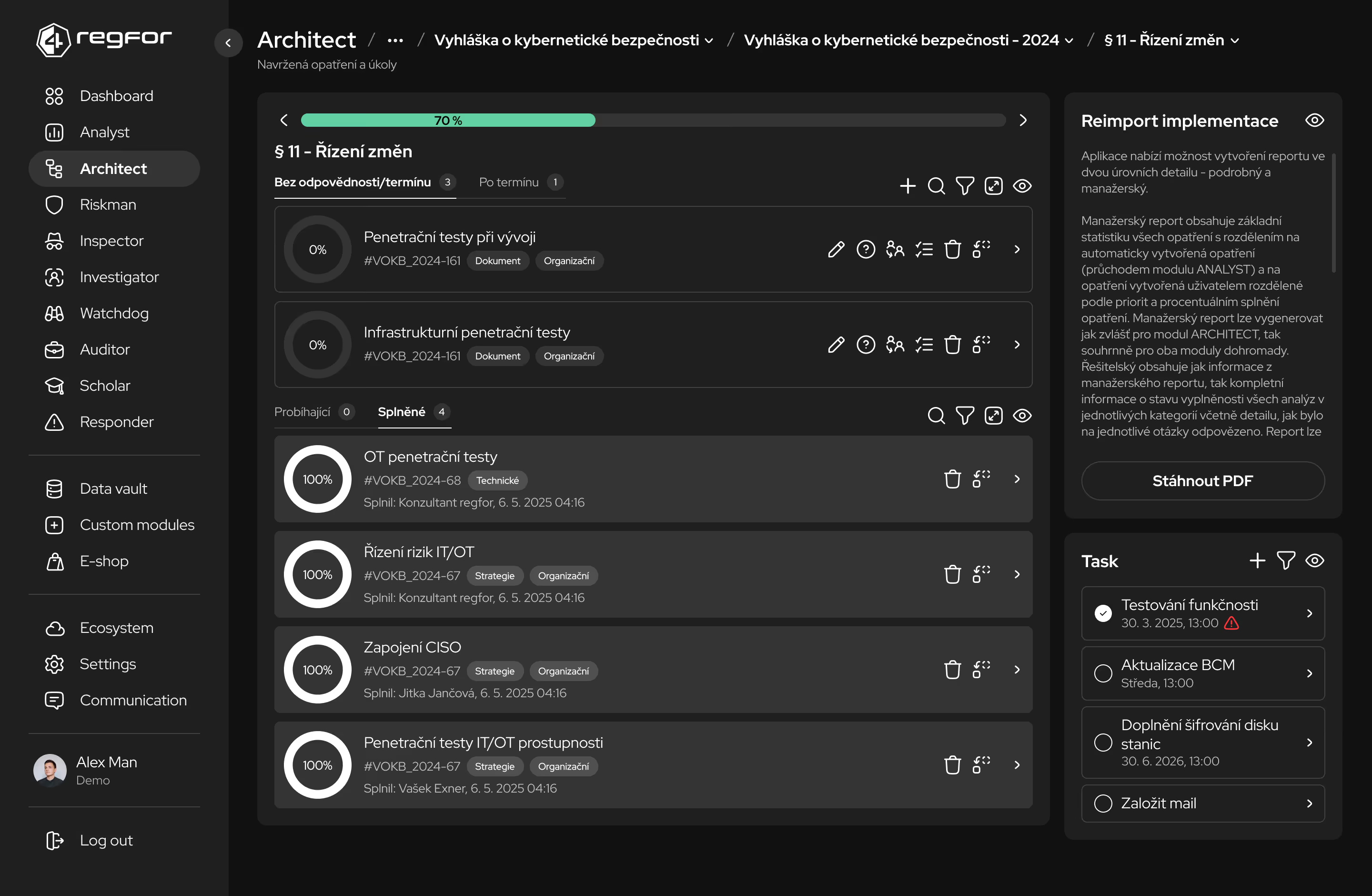
Průběžné kontroly a audity stavu implementace opatření a připravenosti na inspekce.
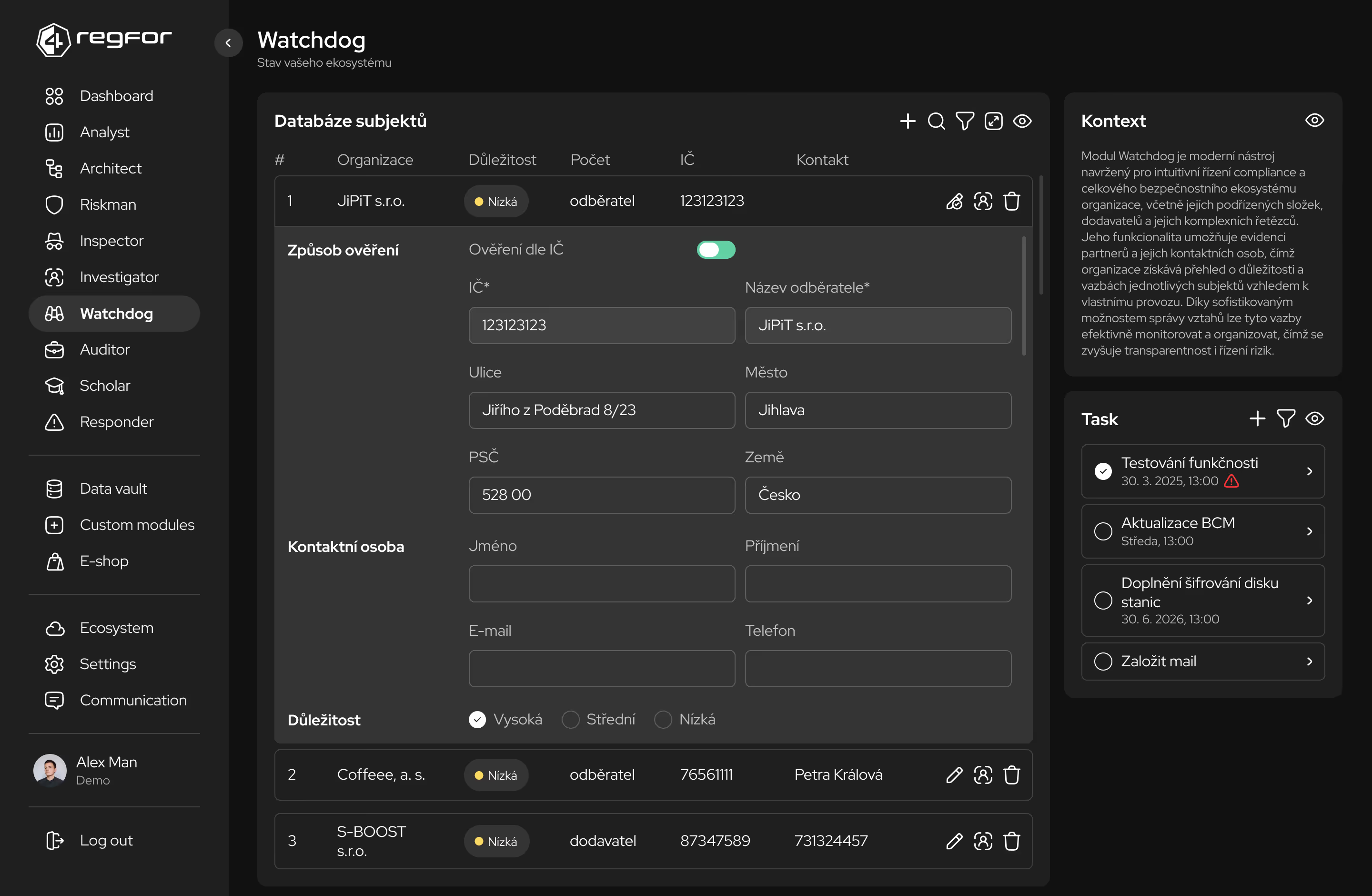
Detailní prověřování dodavatelů s důrazem na řízení rizik dodavatelského řetězce.
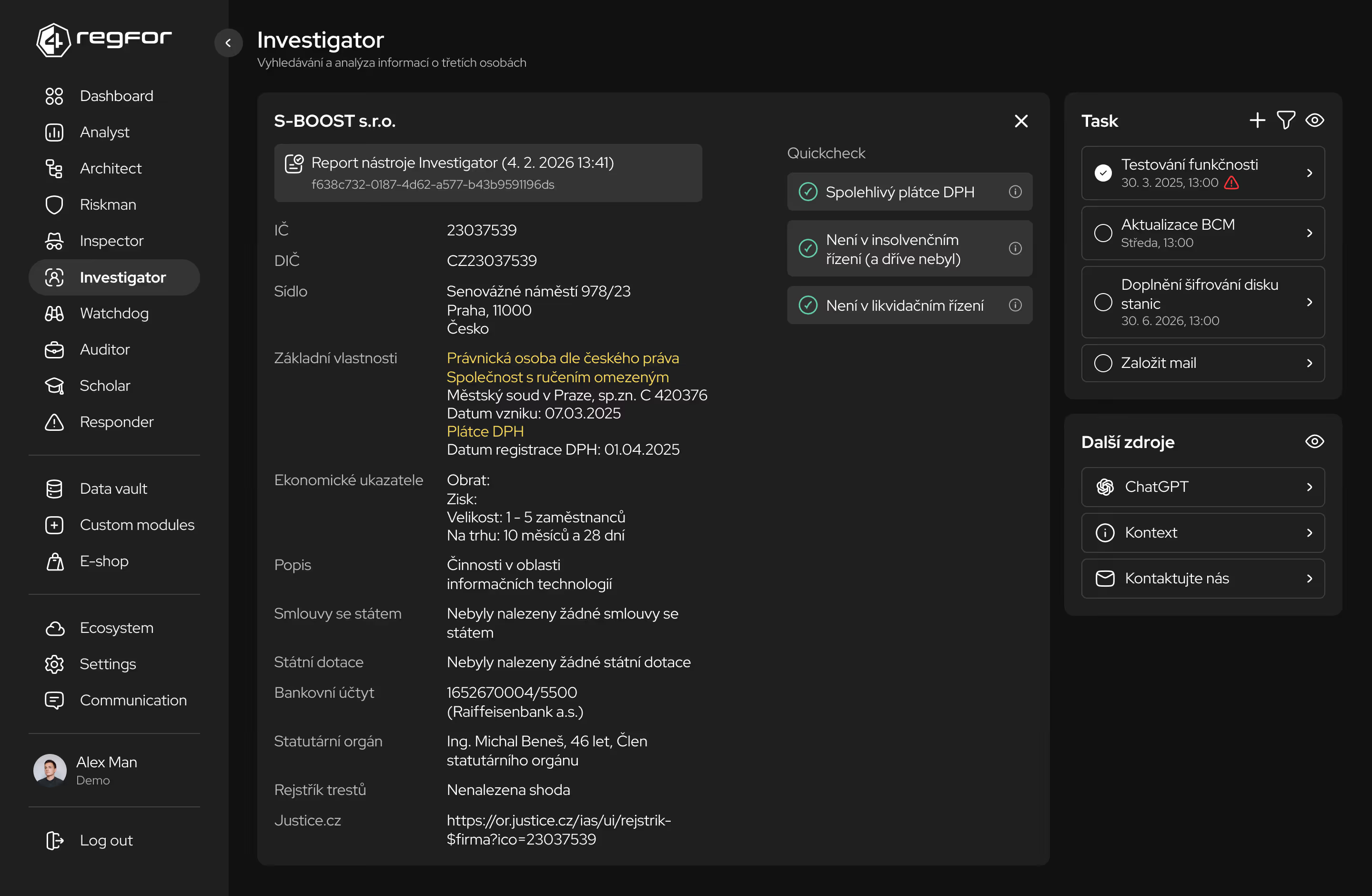
Komplexní řízení rizik včetně hodnocení kritických procesů a závislostí na dodavatelích.
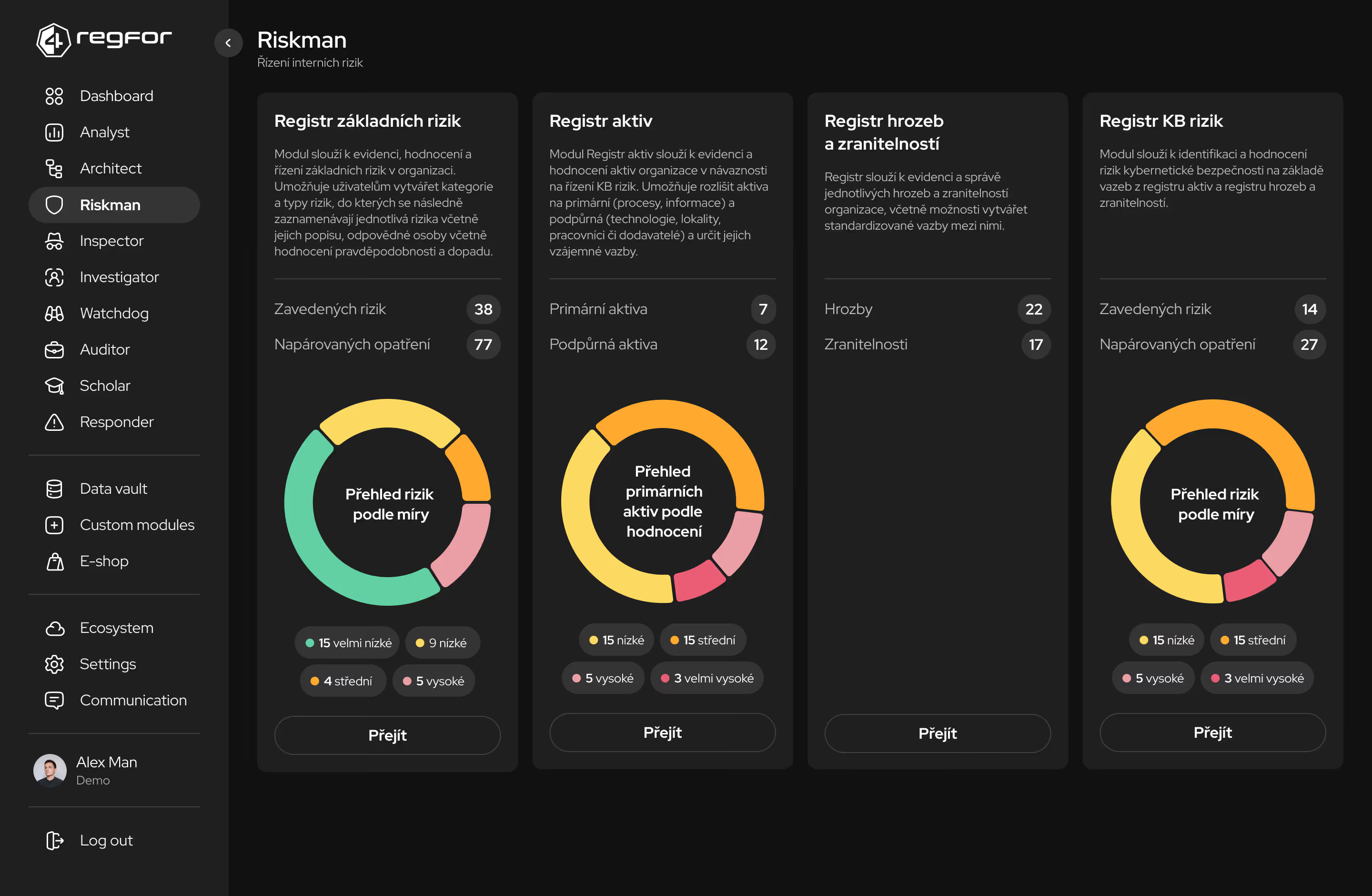
Bezpečné úložiště pro regulatorní dokumentaci a auditovatelné záznamy připravené pro kontroly.
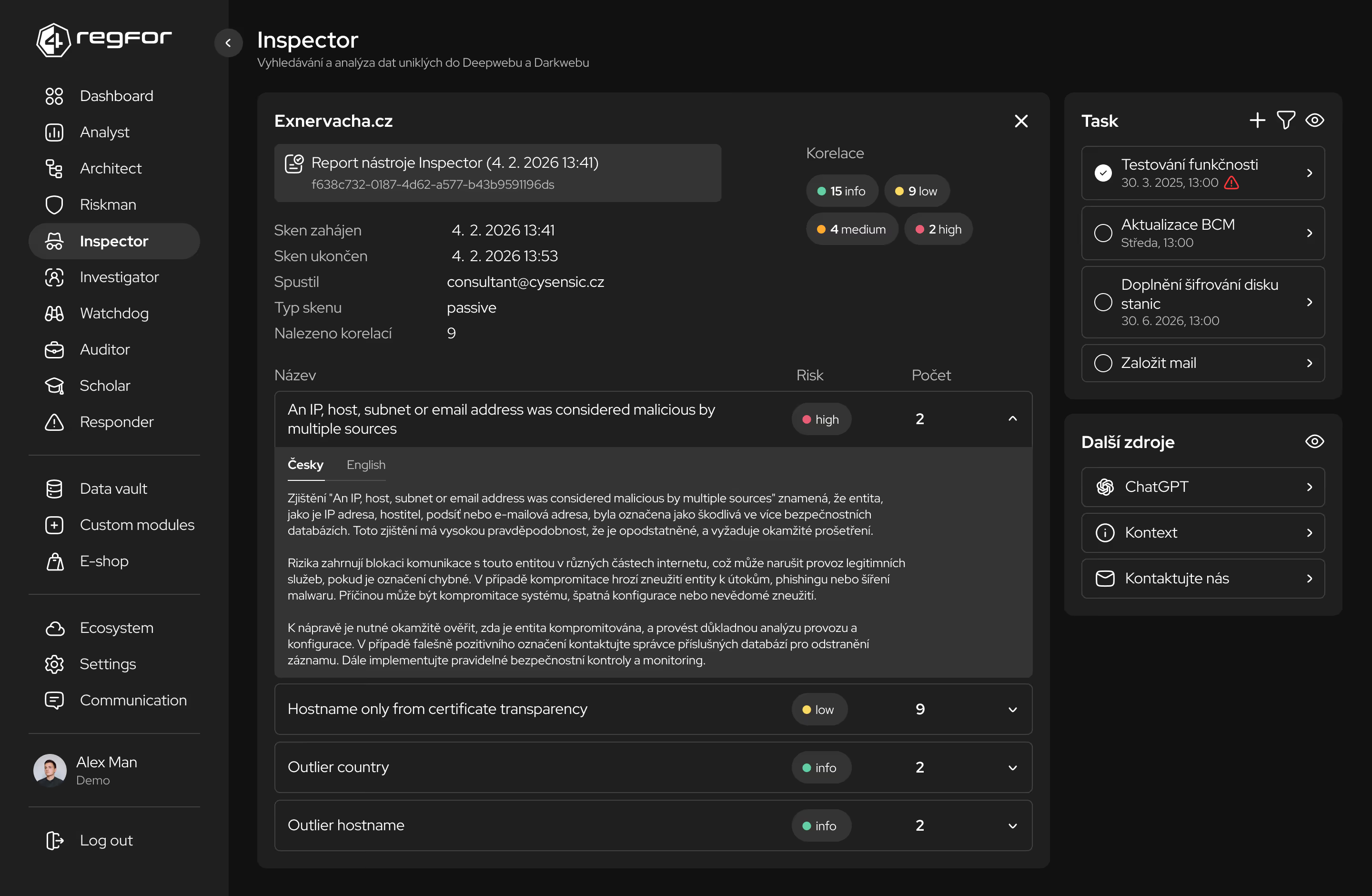
Nepřetržité sledování dodržování požadavků napříč výrobními linkami a laboratořemi.